重磅!20个国内特有品种,迎来评价办法,不重新开展临床试验,国家药监局将不建议使用。
刚刚,国家药品监督管理局药品审评中心发布《国内特有品种评价建议》的通知。


企业应当承担主体责任,根据原总局发布的《总局关于发布仿制药质量和疗效一致性评价品种分类指导意见的通告》(2017年第49号),同时结合附件中的评价建议及相关技术指导原则,对国内特有品种进行深入研究。

根据原食药监总局2017年第49号文件的要求,针对国内特有品种,由企业选择可重新开展临床试验证明其安全有效性,并参照《化学药品仿制药口服固体制剂质量和疗效一致性评价申报资料要求(试行)》提交申请,后续审核通过后视同通过一致性评价。
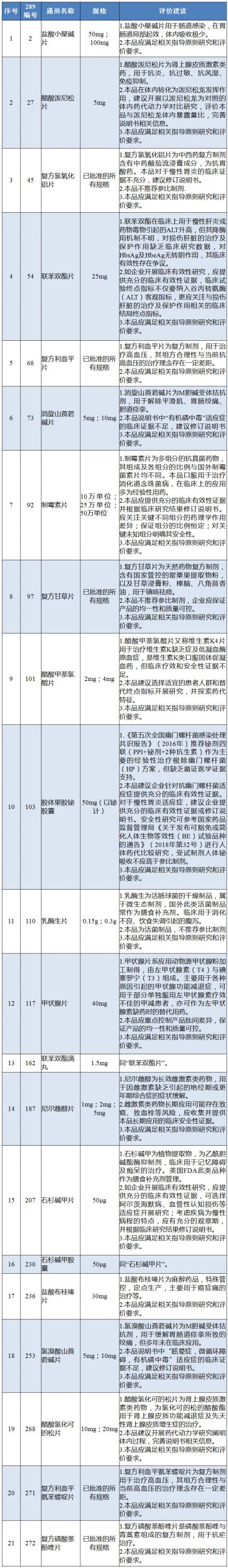
附:国内特有品种评价建议